Latihan 8 :
1. Kelarutan Mg(OH) dalam NaOH 0,1 M dengan Ksp Mg(OH)2 = 1,8 x 10-11 mol-3 L-3 adalah….
a. 1,8 x 10-13 mol/L
b. 1,8 x 10-10 mol/L
c. 4,5 x 10-10 mol/L
d. 1,8 x 10-9 mol/L
e. 6,7 x 10-6 mol/L
Penyelesaian :

2. Larutan jenuh X(OH)2 Memiliki pOH = 5. maka hasil kali kelarutan (Ksp) dari X(OH)2 tersebut….
a. 4 x 10-3
b. 4 x 10-9
c. 2 x 5-12
d. 5 x 10-16
e. 7 x 10-13
Penyelesaian

3. Larutan jenuh senyawa Hidroksida dari suatu logam, M(OH)2 mempunyai Ph = 9 Nilai Ksp (hasil kali kelarutan ) dari senyawa ini adalah….
a. 3,3 x 10-21
b. 3,0 x 10-20
c. 1,0 x 10-10
d. 3,0 x 10-35
e. 3,3 x 10-37
Penyelesaian :

4. Pada suhu tertentu kelarutan PbCl2 dalam air adalah 2,5 x 10-2 Hasil Kali kelarutan (Ksp) PbCl2 adalah….
a. 6,25 x 10-6
b. 6,25 x 10-5
c. 6,25 x 10-4
d. 7,25 x 10-4
e. 7,5 x 10-4
Penyelesaian
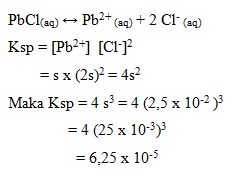
Kuis 8 :
Chapter 13 :
1. Kenaikan suhu akan mempercepat laju reaksi karena …
a. kenaikan suhu akan menyebabkan konsentrasi pereaksi meningkat
b. frekuensi tumbukan semakin tinggi
c. dalam reaksi kimia suhu berperan sebagai katalisator
d. kenaikan suhu akan mengakibatkan turunnya energi aktivasi
e. energi kinetik partikel-partikel yang bereaksi semakin tinggi
Pembahasan :
Kenaikan suhu akan mempercepat laju reaksi dikarenakan energi kinetik partikel-partikel yang bereaksi semakin tinggi. Apabila suhunya menurun maka energi kinetik partikel-partikel yang bereaksi semakin kecil.
2. 1. Berbagai pernyataan sifat-sifat katalis sebagai berikut.
2. Katalis dapat diracuni oleh zatter tentu
3. Katalis hanya diperlukan dalam jumlah sedikit
4. Katalis mempunyai aksi spesifik, artinya hanya dapat menganalisis satu reaksi tertentu
5. Katalis tidak mengalami perubahan yang kekal dalam reaksi, tetapi mungkin terlibat dalam mekanis mereaksi.
Pernyataan yang benar adalah….
a. 1, 2 dan 3
b. 1 dan 3
c. 2 dan4
d. Hanya 4
e. Semua jawaban benar.
Pembahasan :
Dari pertanyaan diatas pertanyaan yang benar yaitu 1,2,3,4 jadi semua jawaban benar yaitu pada obsen e
Chapter 14 :
1. Pada reaksi kesetimbangan CO(g) + H2O(g) ↔ H2(g) + CO2(g) tetapan kesetimbangannya = 1,00.
Banyaknya mol CO yang ditambahkan kedalam 3 mol H2O supaya terbentuk 2 mol H2 dan CO2 adalah . . . .
a. 3 mol
b. 4 mol
c. 4/3 mol
d. ¾ mol
e. 6 mol
Pembahasan :
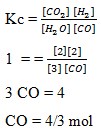
2.Pada temperatur 200 K , harga Kc untuk suatu reaksi kesetimbangan gas adalah
2PQ(g) ↔ P2(g) + Q2(g) adalah 473. Jika R= 0,082 atm mol-1 K-1 maka harga Kp untuk reaksi tersebut adalah . . . .
a. 0,01
b. 100
c. 236,5
d. 473
e. 946
Pembahasan
Diket :
2PQ(g) ↔ P2(g) + Q2(g)
Kc = 473
R = 0,082
T = 200 K
Dn = 0
dit : Kp
Maka :
Kp = Kc (RT)Dn
Kp = 473 (0,082 x 200 )0
Kp = 473 (16,4)0
Kp = 473 (1)
Kp = 473
Chapter 15 :
1. Jika 100 mL lautan HCl 0,01 M dan 100 mL larutan NaOH 0,1 M dicampurkan, maka jumlah garam NaCl (Mr = 58,5) yang terbentuk adalah…..
a. 58,5 mg
b. 57,5 mg
c. 56,5 mg
d. 55,5 mg
e. 585 mg
Pembahasan :
Jumlah mmol NaCl = jumlah mmol HCl
= jumlah mmol NaOH = 10 mmol
Massa NaCl = jumlah mmol NaCl × Mr NaCl
= 10 mmol × 58,5 mg mmol−1 = 585 mg
2. Jika 100 mL larutan BOH 0,1 M memiliki konsentrasi ion OH− yang sama dengan konsentrasi ion OH− dalam 50 mL larutan NaOH 0,001 M, nilai Kb BOH nya adalah…..
a. 10-5
b. 10-4
c. 10-3
d. 10-2
e. 10-1
Pembahasan :
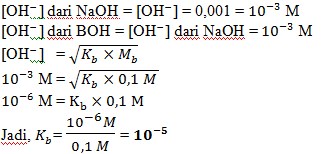
Chapter 16 :
1. Kelarutan Mg(OH) dalam NaOH 0,1 M dengan Ksp Mg(OH)2 = 1,8 x 10-11 mol-3 L-3 adalah….
a. 1,8 x 10-13 mol/L
b. 1,8 x 10-10 mol/L
c. 4,5 x 10-10 mol/L
d. 1,8 x 10-9 mol/L
e. 6,7 x 10-6 mol/L
Penyelesaian :

2. Larutan jenuh X(OH)2 Memiliki pOH = 5. maka hasil kali kelarutan (Ksp) dari X(OH)2 tersebut….
a. 4 x 10-3
b. 4 x 10-9
c. 2 x 5-12
d. 5 x 10-16
e. 7 x 10-13
Penyelesaian

Chapter 17 :
a. oksigen
b. nitrogen
c. hidrogen
d. helium
e. xenon
Pembahasan:
Lapisan atmosfer bumi merupakan campuran dari gas-gas yang tidak tampak dan tidak berwarna. Volume udara kering tersusun oleh empat gas utama yaitu Nitrogen sebanyak 78 %, Oksigen sebanyak 21 %, Argon sebanyak 0,93 %, Karbon dioksida sebanyak 0,03, dan zat-zat lain yang kurang stabil sebanyak 0,04 %.
a. anemometer
b. barometer
c. termometer
d. seismograf
e. pluviometer
Pambahasan:
Anemometer adalah alat yang digunakan untuk mengukur kecepatan angin. Barometer aneroid adalah alat yang digunakan untuk mengukur tekanan udara. Termometer adalah alat yang digunanakan untuk mengukur suhu udara. Seismograf adalah alat yang digunakan untuk mengukur gempa bumi. Pluviometer adalah alat yang digunakan untuk mengukur curah hujan.
Chapter 18 :
1. Pada temperatur tinggi, bila gas karbon monoksida bereaksi dengan gas hydrogen akan menghasilkan methanol seperti pada persamaan reaksi berikut ini.
CO(g) + 2H2(g) ↔ CH3OH(g)
Bila 0,4 mol CO dan 0,30 mol H2 Bereaksi dalam wadah 1 L dan mencapai kesetimbangan ternyata terbentuk 0,06 mol CH3OH. Nilai Kc untuk reaksi tersebut adalah . . . .
a. 0,50
b. 0,98
c. 1,70
d. 2,0
e. 5,4
Pembahasan
Diket :
CO = 0,4 mol
H2 = 0,30 mol
CH3OH = 0,06 mol
Dit : Kc
Penyelesaian :
Kc = [CH3OH] / [H2]2 [CO]
Kc = 0,06 / [0,30]2 [0,40]
Kc = 0,06 / (0,09) (0,4)
Kc = 0,06/0,036
Kc = 1,6667 ~ 1,7
2. Pada suhu tertentu dalam ruang 10 L terdapat Kesetimbangan dari reaksi
2SO3(g) ↔ 2SO2(g) + O2(g)
Apabila 80 gr SO3 (S= 32, O = 16) dipanaskan hingga tercapai keadaan setimbang pada suhu tersebut, didapat perbandingan mol SO3 : O2 = 2: 1 Tetapan Kesetimbangan dari reaksi adalah . . . .
a. 25
b. 2,5
c. 0,4
d. 0,04
e. 0,025
Pembahasan :
Diket : gr SO3 = 80 gr
SO3 : O2 = 2 : 1
V = 10 L
2SO3(g) ↔ 2SO2(g) + O2(g)
Dit : Kc
Penyelesaian :


Tidak ada komentar:
Posting Komentar